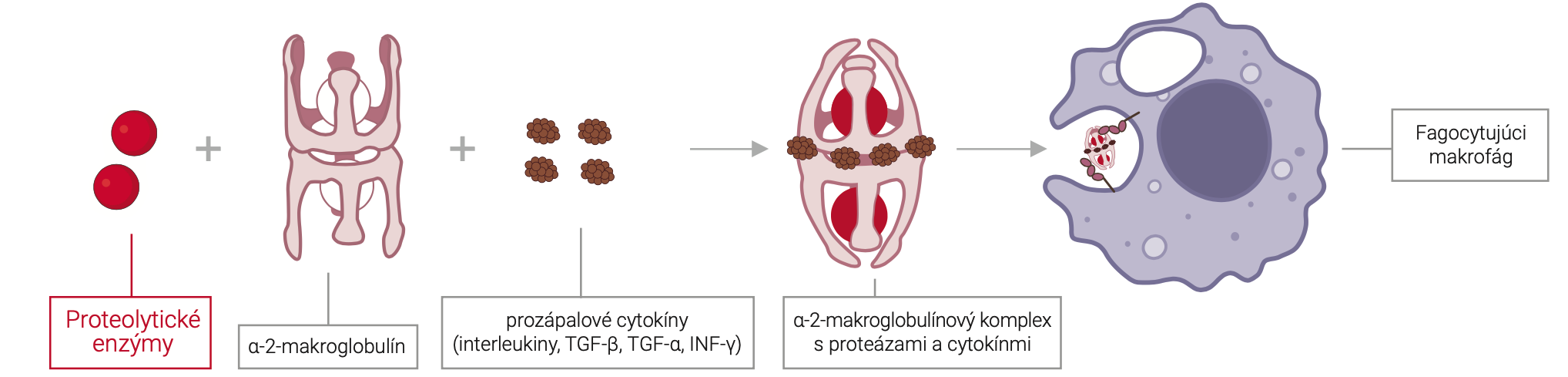
Proteolytické enzýmy zohrávajú dôležitú úlohu pri regulácii zápalu. Odstraňujú prebytočné prozápalové cytokíny, čisté kapiláry a vďaka tzv. vehikulovému efektu prispievajú k lepšej distribúcii antiseptík pri lokálnom použití a antibiotík pri všeobecnom užívaní.
Zápal je prirodzenou reakciou nášho tela na zranenie. Je to základný fyziologický proces, ktorým telo udržuje rovnováhu vnútorného prostredia alebo reaguje na vonkajšie alebo vnútorné poškodenie alebo zranenie. Napríklad v prípade ústnej dutiny ide o reakciu na pôsobenie baktérií obsiahnutých v zubnom plaku. Zápal ďasien sa prejavuje začervenaním, bolesťou a opuchom – to všetko je súčasťou prirodzenej reakcie tela a prirodzeného procesu hojenia. Problém nastáva, keď naše telo vyčerpá svoju schopnosť potlačiť príčinu a vyliečiť poškodené tkanivo prostredníctvom akútnej zápalovej reakcie. V takejto situácii sa zápal zmení na chronické štádium, keď naše telo nastaví imunitnú rovnováhu medzi stále existujúcou príčinou a do istej miery vyčerpanými možnosťami vlastnej obranyschopnosti. Takto vytvorená rovnováha je zvyčajne sprevádzaná deštrukciou tkaniva rôznou rýchlosťou. V ústnej dutine je príkladom takéhoto chronického ochorenia parodontitída (zápal podporných tkanív zuba, pri ktorom už dochádza k trvalému poškodeniu).
Proteolytické enzýmy, známe aj ako proteázy, zohrávajú kľúčovú úlohu v mnohých biologických procesoch vďaka svojej schopnosti štiepiť proteíny na menšie peptidy alebo jednotlivé aminokyseliny. Táto funkcia je kľúčová napríklad pri trávení potravy, kde enzýmy ako pepsín a trypsín pomáhajú rozkladať bielkoviny na jednoduchšie látky, ktoré sa potom môžu absorbovať do tela. Jednou z najdôležitejších funkcií proteolytických enzýmov v tele je regulácia bunkových funkcií. Proteolytické enzýmy zohrávajú kľúčovú úlohu pri obnove tkanív, v bunkovom cykle, ale aj v apoptóze (programovaná bunková smrť). Ich schopnosť špecificky rozkladať proteínové substráty je tiež nevyhnutná pre aktiváciu alebo deaktiváciu mnohých bioaktívnych molekúl, čo umožňuje organizmu rýchlo reagovať na zmeny vo svojom prostredí a udržiavať homeostázu. V neposlednom rade zohrávajú proteolytické enzýmy dôležitú úlohu pri regulácii zápalovej reakcie tela na vonkajšie alebo vnútorné zranenie. Medzi dôležité proteolytické enzýmy s imunomodulačným účinkom patria trypsín, chymotrypsín, bromelaín a papaín.
Bromelaín je proteolytický enzým, ktorý je známy svojimi výraznými protizápalovými vlastnosťami. Bromelaín má schopnosť modulovať zápalové procesy v tele prostredníctvom niekoľkých rôznych mechanizmov. Jedným z hlavných spôsobov, ako bromelaín pôsobí protizápalovo, je jeho schopnosť rozkladať bielkoviny v mieste zápalu, čo vedie k zníženiu opuchu a bolesti. Bromelaín špecificky hydrolyzuje fibrín a redukuje plazmatický fibrinogén, čo pomáha znižovať opuch spojený so zápalom (Kelly, 1996; Varilla a kol., 2021). Okrem toho štúdie ukázali, že bromelaín môže inhibovať agregáciu krvných doštičiek, čo znižuje riziko trombózy v miestach zápalového poškodenia (Glaeser et al., 2006). Bromelaín tiež pôsobí na imunitný systém moduláciou aktivity bielych krviniek, najmä makrofágov a T-buniek. Ukázalo sa, že bromelaín znižuje expresiu adhéznych molekúl na povrchu leukocytov, čo obmedzuje ich migráciu do miest zápalu, a tým znižuje celkovú zápalovú odpoveď (Hale et al., 2002). Tento enzým ovplyvňuje aj produkciu cytokínov, ktoré sú kľúčovými mediátormi zápalu. Napríklad bromelaín znižuje hladiny prozápalových cytokínov, ako je faktor nekrózy nádoru alfa (TNF-α) a interleukín-6 (IL-6), čo ďalej prispieva k zmierneniu zápalových reakcií. Celkovo má bromelaín široké spektrum protizápalových účinkov, ktoré sú spôsobené jeho proteolytickou aktivitou, moduláciou imunitnej odpovede a schopnosťou ovplyvňovať zápalové signálne dráhy. Jeho využitie pri liečbe zápalových stavov je preto sľubné, najmä pri liečbe opuchov, bolesti a iných zápalových príznakov (Pavan et al., 2012).
Trypsín a chymotrypsín sú serínové proteázy, ktoré sú známe nielen svojimi tráviacimi funkciami, ale aj výraznými protizápalovými účinkami. Oba enzýmy zohrávajú kľúčovú úlohu pri regulácii zápalových procesov, čo je dôležité pri liečbe rôznych zápalových ochorení.
Trypsín je endopeptidáza, ktorá rozkladá proteíny na kratšie peptidy, čo pomáha nielen pri trávení, ale aj pri modulácii imunitnej odpovede. Jedným z mechanizmov protizápalového účinku trypsínu je jeho schopnosť inaktivovať proteíny zapojené do zápalových reakcií, ako sú cytokíny a chemokíny (spolu s bromelaínom). Inaktiváciou týchto molekúl trypsín znižuje migráciu zápalových buniek na miesto zápalu, čo vedie k zníženiu zápalovej reakcie. Tento účinok trypsínu pomáha znižovať poškodenie tkaniva počas zápalu. Pozitívny protizápalový účinok trypsínu sa pripisuje aj jeho fibrinolytickej aktivite, nazývanej fibrinolýza, ktorá je dôležitá pre rýchlejšie uvoľňovanie mikrocirkulácie a následné odstránenie toxických metabolitov a dodanie imunokompetentných látok do miesta zápalu (Shah a Mital, 2018).
Jedným z mechanizmov, ktorými trypsín prispieva k zníženiu zápalových reakcií, je jeho schopnosť aktivovať alfa-2-makroglobulín (α2M), veľký plazmatický proteín, ktorý funguje ako inhibítor proteázy, ako aj transportér pre rôzne molekuly vrátane cytokínov.
Alfa-2-makroglobulín (α2M) má jedinečnú štruktúru, ktorá mu umožňuje zachytávať a inaktivovať širokú škálu cytokínov, čo sú malé proteíny, ktoré zohrávajú kľúčovú úlohu v signalizácii počas imunitnej odpovede a zápalu (Borth, 1992). Aktivácia α2M trypsínom vedie k tomu, že α2M viaže prozápalové cytokíny, ako je faktor nekrózy nádoru alfa (TNF-α) a interleukín-6 (IL-6), čím sa znižuje ich biologická dostupnosť a obmedzujú ich účinky na zápalové miesta. Tento proces významne prispieva k regulácii zápalových reakcií, pretože znižuje koncentráciu voľných cytokínov. Tieto cytokíny by inak podporovali a udržiavali zápalový stav. Okrem toho by ich nadmerné množstvo viedlo k chronickému zápalu. Keď α2M viaže tieto cytokíny, rýchlo sa vylučujú z obehu prostredníctvom α2M receptorov na povrchu makrofágov a iných buniek imunitného systému. Tento mechanizmus zaisťuje účinné odstránenie prebytočných alebo škodlivých cytokínov z tela, čo ďalej znižuje zápalové procesy a prispieva k regenerácii organizmu po úraze alebo poškodení (Vandooren et al., 2021).
Stručne povedané, trypsín aktivuje alfa-2-makroglobulín na podporu eliminácie prozápalových cytokínov, čo je dôležitý mechanizmus na kontrolu a obmedzenie zápalových reakcií v tele. Tento proces nielenže zabraňuje nadmernej zápalovej reakcii, ale podporuje aj rýchlejší návrat do fyziologickej rovnováhy.
Chymotrypsín tiež vykazuje významné protizápalové účinky, ktoré sa čiastočne prekrývajú, ale tiež sa líšia od funkcií trypsínu. Chymotrypsín je známy svojou schopnosťou rozkladať proteínové substráty aromatickými aminokyselinami, čo umožňuje rozklad špecifických zápalových mediátorov. Štúdie napríklad ukázali, že chymotrypsín môže rozkladať fibrinogén a fibrín, čo pomáha znižovať tvorbu zrazenín a zápalových ložísk. Okrem toho môže chymotrypsín inhibovať aktiváciu určitých receptorov bunkového povrchu, ako je receptor pre faktor aktivujúci krvné doštičky (PAF), ktorý hrá kľúčovú úlohu v zápalových procesoch. Blokovaním aktivácie týchto receptorov prispieva chymotrypsín k zníženiu produkcie zápalových mediátorov a znižuje zápalovú reakciu (Pidard et al., 1991).
Celkovo majú proteolytické enzýmy trypsín, chymotrypsín a bromelaín dôležité protizápalové funkcie, ktoré súvisia s ich schopnosťou degradovať proteíny zapojené do zápalových procesov a modulovať imunitnú odpoveď.
Proteolytické enzýmy v medicíne. Schopnosť proteolytických enzýmov ovplyvňovať zápalové procesy v tele je v medicíne známa už viac ako storočie. Proteolytické enzýmy sa vďaka svojim protizápalovým a imunomodulačným vlastnostiam stali dôležitou súčasťou rôznych terapeutických postupov vrátane liečby športových zranení, chirurgických zákrokov a chronických zápalových ochorení. Ich využitie je rozšírené a ich ďalší potenciál v oblasti medicíny sa stále skúma. Tie sa vo veľkej miere používajú v rôznych klinických aplikáciách a pacienti ich dobre znášajú, ak sa podávajú systémovo a lokálne, takmer bez vedľajších účinkov (Shah et al., 2018). Proteázy prvýkrát systematicky skúmali v polovici 20. storočia česko-nemecký lekár Max Wolf a americká lekárka Helena Benitez, ktorí pozorovali ich priaznivé účinky pri liečbe pacientov s agresívnymi zápalmi a nádormi. Protizápalový potenciál proteáz sa prvýkrát naplno využil počas olympijských hier v Los Angeles, kde nemeckí športovci počas rekonvalescencie používali produkty s proteolytickými enzýmami. Približne pred 30 rokmi boli proteázy schválené Medzinárodnou organizáciou pre kategorizáciu liekov na lekárske použitie ako protizápalové enzýmy (skupina M09AB) pre ich účinnosť pri inhibícii nadmernej aktivácie prozápalových cytokínov a znižovaní ich sekrécie v už stimulovaných imunitných bunkách (IFN-γ, TNF-α, IL1-β, TGF-β), potláčaní hyperaktívnych imunitných buniek, ako sú neutrofilné granulocyty, a indukcii zvýšenia fagocytózy v zápalovom tkanive, čo vedie k rýchlejšiemu odstráneniu nečistôt a patogénov. Dnes sa proteázy používajú vo forme lokálnej terapie ústnej dutiny pre ich trombolytické a protiedémové účinky, ich schopnosť normalizovať, ale nie potláčať imunitnú odpoveď na zápal (Manhart et al., 2002; Lehmann a kol., 1996; Fitzhugh a kol., 2008). V neposlednom rade majú proteolytické enzýmy schopnosť zvyšovať biologickú dostupnosť antibiotík a antiseptík pri spoločnej aplikácii (UPV 308891).
Proteolytické enzýmy v zubnom lekárstve. V zubnom lekárstve našli proteolytické enzýmy od druhej polovice 20. storočia širšie uplatnenie, najmä pre svoj potenciál skrátiť čas hojenia a zvládnuť pooperačné príznaky, ako sú opuchy a bolesť. Štúdie ukázali, že tieto enzýmy môžu byť účinné pri znižovaní pooperačného opuchu a bolesti, najmä po orálnych operáciách, ako je extrakcia tretích stoličiek. Použitie proteolytických enzýmov sa porovnáva s tradičnými protizápalovými liekmi, ako je diklofenak. Proteolytické enzýmy preukázali porovnateľnú účinnosť pri kontrole pooperačných následkov, ako sú opuchy a bolesť po zubnom chirurgickom zákroku alebo po operácii tretieho stolička (Maurer et al., 2001; Majid a Al-Mashhadani, 2014).
Proteolytické enzýmy (proteázy) vďaka svojej biologickej minimálnej invazívnosti nenarúšajú fyziologické procesy na slizniciach a ďasnách ústnej dutiny, zlepšujú ich imunitu a podporujú ich hojenie, znižujú krvácanie a opuchy a tiež znižujú rast baktérií a zubného plaku. Tieto účinky sú zabezpečené najmä optimalizáciou priebehu zápalovej reakcie a jej rozsahu, zlepšením mikrocirkulácie krvi alebo lymfy a imunomodulačným účinkom v zápalom postihnutom tkanive.
Zlepšenie mikrocirkulácie je spôsobené znížením opuchu a proteolytickou aktivitou proteáz, čo umožňuje degradáciu mikrotrombov v krvných kapilárach a proteínových zátok v lymfatických cievach.
Zápal v ústnej dutine a parodontitída. V patofyziológii zápalových ochorení ústnej dutiny zohrávajú úlohu všetky všeobecné znaky zápalu, kde dôležitú úlohu zohrávajú zápalové mediátory, ako sú matricové metaloproteinázy (MMP) a prozápalové cytokíny. Tieto molekuly reagujú na prítomnosť a prienik zubného plaku. Parodontitída je závažné chronické zápalové ochorenie ďasien a podporných tkanív zubov, ktoré môže viesť k postupnej strate zubov, ak sa nelieči adekvátne. Toto ochorenie sa vyvíja zo zápalu ďasien, formy akútneho zápalu ďasien. Zatiaľ čo zápal ďasien postihuje iba ďasná a je zvyčajne reverzibilný pri správnej ústnej hygiene a starostlivosti, parodontitída postihuje hlbšie štruktúry vrátane alveolárnej kosti, parodontálnych väzov a cementu zuba. Vývoj parodontitídy je zložitý proces, ktorý zahŕňa niekoľko etáp. Spočiatku sa zápal ďasien vyskytuje v dôsledku hromadenia zubného plaku, čo je biofilm zložený z baktérií, zvyškov potravy a slín. Ak sa plak neodstraňuje pravidelne, začne mineralizovať a vytvára zubný kameň, ktorý je pevne pripevnený k povrchu zuba. Zubný kameň tiež podporuje rast baktérií, ktoré produkujú toxíny a enzýmy, ktoré poškodzujú ďasná a podporné tkanivá. Ako zápal postupuje, začína deštrukcia parodontálnych väzov a alveolárnej kosti, čo vedie k tvorbe parodontálnych vačkov medzi ďasnom a zubom. Tieto vrecká sa stávajú rezervoármi patogénnych baktérií, ktoré podporujú ďalšiu deštrukciu tkanív a zápal. V pokročilých štádiách parodontitídy dochádza k výraznej strate kosti, čo môže viesť k pohyblivosti zubov a následnej strate (Kinane et al., 2017; Pihlstrom a kol., 2005).
Parodontitída je charakterizovaná akútnym aj chronickým zápalom. Akútny zápal je zvyčajne rýchla reakcia imunitného systému na infekciu bakteriálnymi patogénmi v zubnom plaku. Tento zápal je často sprevádzaný bolesťou, opuchom, začervenaním a krvácaním ďasien. Počas akútnej fázy dochádza k intenzívnemu náboru neutrofilov a makrofágov do postihnutej oblasti, čo je imunitná odpoveď zameraná na elimináciu infekčných agens a zabránenie ich šírenia. Chronický zápal je dlhodobý a môže pretrvávať aj po ústupe akútnej fázy, ak sa neodstránia príčinné faktory, ako je zubný kameň a plak. Chronický zápal je charakterizovaný pokračujúcim poškodením tkaniva v dôsledku pretrvávania bakteriálnej infekcie a imunologickej reakcie hostiteľa. Makrofágy, lymfocyty a plazmatické bunky dominujú v chronickej fáze a produkujú cytokíny, ktoré podporujú zápalovú reakciu a deštrukciu tkaniva. Prítomnosť chronického zápalu môže viesť k nezvratným zmenám v štruktúre parodontálnych tkanív vrátane resorpcie alveolárnej kosti, čo zvyšuje riziko straty zubov. Celkovo je parodontitída výsledkom nepretržitého cyklu akútneho a chronického zápalu, ktorý vedie k postupnému poškodeniu podporných tkanív zubov. Zvládnutie parodontitídy si vyžaduje nielen odstránenie patogénneho biofilmu a zubného kameňa, ale aj kontrolu zápalovej reakcie, aby sa zabránilo ďalšiemu poškodeniu tkaniva a podporilo hojenie tkanív. Liečba môže zahŕňať mechanické čistenie, použitie antimikrobiálnych látok, chirurgický zákrok a v niektorých prípadoch systémovú terapiu na moduláciu imunitnej odpovede (Tonetti et al., 2018; Hajishengallis, 2015; Van & Kornman, 2008).
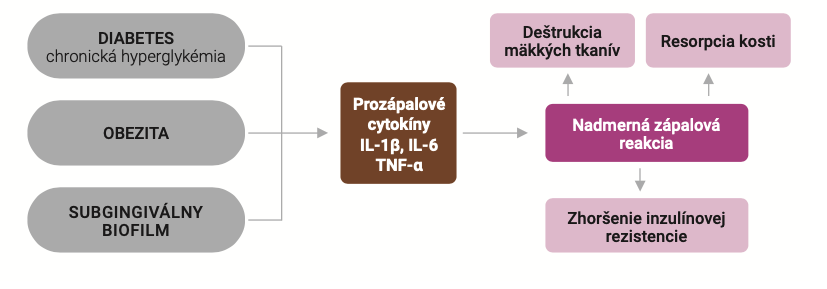
Parodontitída a metabolický syndróm. Parodontitída je šiestou preukázanou komplikáciou cukrovky. Cukrovka je jedným z ochorení metabolického syndrómu. Centrálna obezita v bruchu, inzulínová rezistencia, hyperglykémia (zvýšená hladina glukózy), hypertenzia (vysoký krvný tlak) a dyslipidémia (vysoká hladina triglyceridov a nízky HDL cholesterol) sa významne podieľajú na rozvoji cukrovky. Kombinácia zápalu v ústnej dutine a celkovej cukrovky môže viesť k nadmernej obrannej reakcii, pri ktorej sa uvoľňuje nadmerné množstvo prozápalových cytokínov alebo môže dôjsť k narušeniu rovnováhy medzi prozápalovými a protizápalovými cytokínmi. V dôsledku toho to vedie k celkovej dysregulácii obrannej odpovede v ústnej dutine. Kľúčovými faktormi spájajúcimi parodontitídu a cukrovku sú kľúčové prozápalové cytokíny IL-1, IL-6 a TNF-α. Podobný vzťah existuje medzi IL-6, obezitou a parodontitídou. Výsledky štúdií ukazujú, že zvýšené hladiny TNF-α a IL-6 pochádzajú z tukového tkaniva a zápalového procesu v parodontálnych tkanivách (Smyth a Heron, 2006).
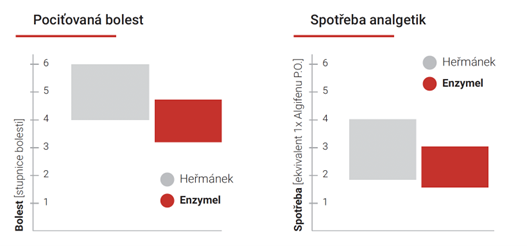
Proteolytické enzýmy pri liečbe pooperačných rán v horných dýchacích cestách. Hojenie pooperačných rán v horných dýchacích cestách je často veľmi ťažké a bolestivé kvôli neustálej prítomnosti potravy a baktérií, pohybu pri rozprávaní a neustálej prítomnosti agresívnych slín. Na väčšine chirurgických oddelení sa používajú prírodné roztoky, najmä s harmančekom, na urýchlenie hojenia a odstránenie pooperačných problémov pacienta. V klinickom skúšaní bol použitý mukoadhezívny gél obsahujúci proteolytické enzýmy trypsín a chymotrypsín. V skupine 80 pacientov boli získané empirické a dotazníkové údaje na porovnanie účinnosti skúmaných látok, najmä v oblasti vnímanej bolesti, komfortu prehĺtania, dĺžky hospitalizácie, výskytu komplikácií a konzumovaných analgetík. Získané výsledky ukázali zníženie spotreby analgetík, zníženie bolesti a zvýšenie komfortu pacienta pri použití mukoadhezívneho gélu s obsahom proteolytických enzýmov (Šimurdová, 2021).
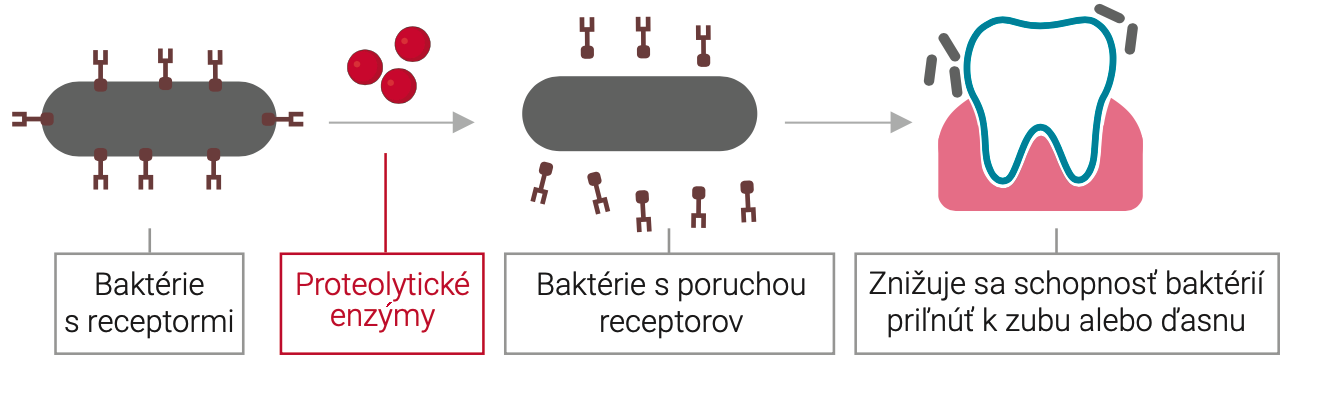
Proteolytické enzýmy a zubný plak. Baktérie v ústach musia priľnúť k sklovine, aby prežili, a potom vytvoriť hlienovitý obal (biofilm), ktorý im poskytuje ochranu a vhodné prostredie na množenie. Na priľnutie k sklovine používajú fimbriu, čo sú proteíny, ktoré slúžia ako kotvy na pripojenie baktérií. Akonáhle sa baktérie prichytia na sklovinu, začnú vytvárať ochranný obal podobný hlienu. Táto biofilmová sieť je komplexná zmes exopolysacharidov, proteínov, nukleových kyselín a lipidov, ktorá poskytuje mechanickú stabilitu a chráni baktérie pred antimikrobiálnymi látkami a imunitným systémom. Proteolytické enzýmy bromelaín a trypsín zohrávajú dôležitú úlohu pri inhibícii bakteriálnej adhézie k zubnej sklovine, čo je kľúčový krok v prevencii tvorby plaku a súvisiacich ochorení ústnej dutiny, ako je zubný kaz, zápal ďasien a parodontitída. Proteolytické enzýmy rozkladajú proteíny v biofilme a proteínových fimbriách, najmä tie, ktoré sú nevyhnutné pre bakteriálnu priľnavosť k sklovine a ďasnám. Týmto spôsobom proteolytické enzýmy narúšajú schopnosť baktérií pevne sa prichytiť na povrch zubov, čím znižujú bakteriálnu kolonizáciu a riziko tvorby plaku. V dôsledku toho sa zvyšuje citlivosť baktérií a biofilmu na mechanické odstránenie počas čistenia zubov (Chakraborty et al., 2021; Huang a kol., 2024).
Chlórhexidín je zlatým štandardom v zubnom lekárstve. Chlórhexidín je jednou z látok s antiseptickým účinkom. Antiseptiká pôsobia nešpecifickým mechanizmom proti širokému spektru baktérií G+ a G-, plesní, vírusov a kvasiniek. Chlórhexidín pôsobí na bakteriálnu stenu nešpecifickým spôsobom, narúša osmotickú rovnováhu bunkovej steny a cytoplazmatickej membrány vytváraním neselektívnych pórov aj pri nízkych koncentráciách. Cytoplazmatická tekutina následne uniká cez tieto póry a dochádza k nekróze buniek. Vďaka svojim veľmi dobrým antibakteriálnym účinkom bol chlórhexidín zaradený do modelového zoznamu základných liekov WHO Svetovou zdravotníckou organizáciou. V zubnom lekárstve sa chlórhexidín používa hlavne pre svoju schopnosť inhibovať tvorbu plaku a potláčať rozvoj zápalu ďasien (zápal ďasien, parodontitída) v ústnej dutine (Jones, 1997). Chlórhexidín má široké využitie na ošetrenie slizníc alebo mäkkých tkanív ako antiseptikum u ľudí aj zvierat, zatiaľ čo na krátkodobé použitie, napríklad v ústnej dutine, sa chlórhexidín používa ako:
1) doplnok na mechanické odstránenie zubného plakuu pri čistení zubov a odborná profylaxia na udržanie správnej ústnej hygieny;
2) starostlivosť po operácii ústnej dutiny, vrátane parodontálnej chirurgie alebo koreňovej chirurgie;
3) ako okamžitý profylaktický prostriedok pri prevencii bakteriémie po extrakcii;
4) liek na opakované ulcerácie v ústnej dutine;
5) zariadenie na liečbu stomatitídy spôsobenej zubnými protézami a na ošetrenie suchých lôžok;
6) prostriedok pri liečbe infekcie ústnej dutiny a akútneho nekrotizujúceho ulcerózneho zápalu ďasien.
Chlórhexidín sa používa v zubnom lekárstve ako lokálne antiseptikum v koncentrácii 0,12% a vyššej, čo má za následok množstvo vedľajších účinkov. Hlavným lokálnym vedľajším účinkom chlórhexidínu pri použití v zubnom lekárstve je exogénne tmavé zafarbenie zubov. Už po niekoľkých dňoch užívania chlórhexidínu sa na vlastných zuboch a umelých zuboch objavia tmavožlté alebo hnedé škvrny. Intenzita farbenia súvisí najmä s koncentráciou použitého chlórhexidínu a rozdielmi v štruktúre skloviny u jednotlivých pacientov. Medzi ďalšie vedľajšie účinky patrí dočasné zhoršenie vnímania chuti, chuťové poháriky na vnímanie slanej chuti sú ovplyvnené v najväčšej miere. Príležitostne sú hlásené prípady pálenia a tvorby bolestivých lézií na sliznici ústnej dutiny, ktoré sa javia ako idiosynkratická reakcia a závisia od použitej koncentrácie. Samotný chlórhexidín má horkú chuť, ktorú je veľmi ťažké maskovať. Okrem toho sa môže vyskytnúť podráždenie ústnej dutiny s lokálnymi príznakmi alergie.
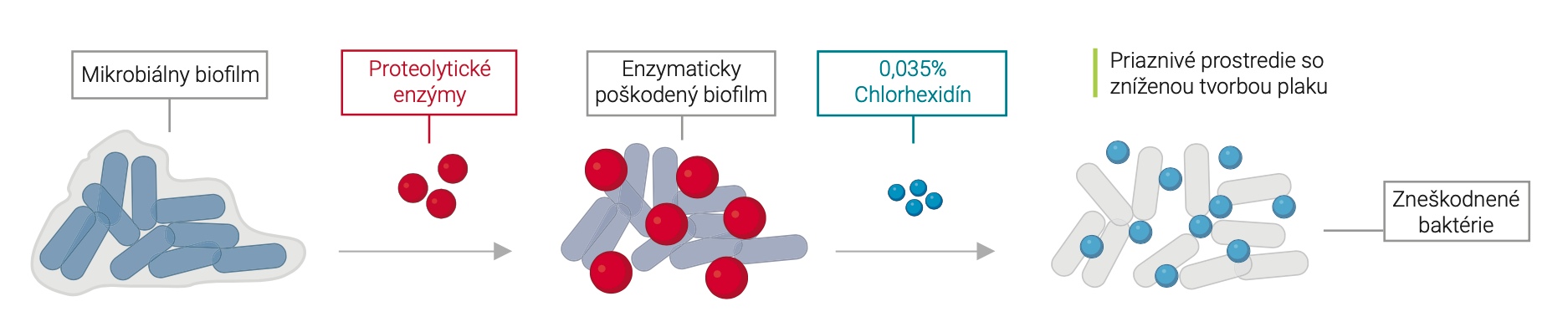
Vďaka kombinácii chlórhexidínu s proteolytickými enzýmami je možné účinne znížiť koncentráciu chlórhexidínu na 0,035% pri zachovaní rovnakej antimikrobiálnej aktivity ako koncentrácia samotného chlórhexidínu 4-krát vyššia (0,12 – 0,15%), ale s eliminovanými vedľajšími účinkami. Tento účinok sa používa vo výrobkoch na humánne a veterinárne použitie (Enzymel® a Venzymel®).
Úloha farmaceuta v starostlivosti o ústnu dutinu. Lekárnici a asistenti v lekárni zohrávajú dôležitú úlohu v starostlivosti o pacientov so zápalom v ústnej dutine. Pri návšteve lekárne môžu pacienti s pretrvávajúcim zápalom alebo sklonom k zápalu (diabetes mellitus, pacienti s oslabenou imunitou) získať informácie o vhodných produktoch, ktoré môžu pomôcť zlepšiť stav zubov, ďasien a ústnej sliznice. Prevencia problémov v ústnej dutine je rovnako dôležitá ako v iných oblastiach ľudského zdravia. Lekárnici môžu pacientom vysvetliť dôležitosť pravidelných návštev zubára, správne techniky čistenia zubov a medzizubných priestorov a dôležitosť vyváženej stravy. Lekárnici a pracovníci v lekárni sú dôležitými členmi zdravotníckeho tímu, ktorý sa stará o zdravie pacientov.
Záverom možno povedať, že proteolytické enzýmy predstavujú významný pokrok v starostlivosti o zuby, ďasná a sliznice. Zápal je prirodzenou obrannou reakciou tela na zranenie alebo infekciu, ale ak pretrváva, môže viesť k chronickým ochoreniam, ako je parodontitída, ktorá je charakterizovaná deštrukciou podporných tkanív zuba a môže viesť k strate zubov. Proteolytické enzýmy majú schopnosť rozkladať prebytočné prozápalové cytokíny, ktoré sú zodpovedné za udržanie zápalového stavu a jeho prechod do chronického štádia. Komorbidity, ako je cukrovka, majú negatívny vplyv na imunitný systém a môžu zhoršiť priebeh zápalu v ústnej dutine, čím sa zvyšuje riziko závažných komplikácií, ako je parodontitída. Okrem toho proteolytické enzýmy narúšajú štruktúru bakteriálneho biofilmu (zubného plaku) rozkladom proteínov a polysacharidov, ktoré tvoria jeho ochranný obal. To znižuje schopnosť baktérií priľnúť k povrchu zubov a ďasien a zvyšuje ich citlivosť na antimikrobiálne látky. To je výhodné najmä po zubných zákrokoch, ako sú operácie alebo extrakcie zubov, kedy je dôležité minimalizovať riziko infekcií a podporiť rýchle a bezproblémové hojenie.
Lokálne aplikované proteolytické enzýmy vo forme prípravkov na domáce použitie (zubná pasta, gél) ponúkajú inovatívne riešenie pre ústnu hygienu nielen pri zápalových stavoch. Zlepšujú ústnu hygienu a zvyšujú komfort pacienta, čo je kľúčové pre dlhodobé udržanie zdravia ústnej dutiny.
CITÁCIE
- Borth, W. (1992). „Alpha 2-macroglobulin, a multifunctional binding protein with targeting characteristics.“ FASEB Journal, 6(15), 3345-3353.
- Chakraborty AJ, et al. (2021). „Bromelain a Potential Bioactive Compound: A Comprehensive Overview from a Pharmacological Perspective.“ Life (Basel), 11(4).
- Fitzhugh, D.J., et al. (2008). „Bromelain treatment decreases neutrophil migration to sites of inflammation.“ Clin Immunol, 128(1).
- Hajishengallis, G. (2015). „Periodontitis: from microbial immune subversion to systemic inflammation.“ Nature Reviews Immunology, 15(1), 30-44.
- Huang, Y., Han, Q., Zhou, J. et al. (2024). „The effect of bovine trypsin on dental biofilm dispersion: an in vitro study.“ Odontology, 112, 501–511.
- Jones, C.G. (1997). „Chlorhexidine: is it still the gold standard?“ Periodontol 2000, 15, 55-62.
- Gläser D, Hilberg T. „The influence of bromelain on platelet count and platelet activity in vitro.“ Platelets. 2006 Feb;17(1):37-41.
- Hale LP, Greer PK, Sempowski GD. „Bromelain treatment alters leukocyte expression of cell surface molecules involved in cellular adhesion and activation.“ Clin Immunol. 2002 Aug;104(2):183-90.
- Kelly, G.S., et al. (1996). „Bromelain: a literature review and discussion of its therapeutic applications.“ Alt Med Rev 1996;1(4):243-257.
- Kinane, D. F., Stathopoulou, P. G., & Papapanou, P. N. (2017). „Periodontal diseases.“ Nature Reviews Disease Primers, 3.
- Lehmann, P.V. (1996). „Immunomodulation by proteolytic enzymes.“ Nephrol Dial Transplant, 11(6).
- Majid, O.W., Al-Mashhadani, B.A. (2014). „Perioperative bromelain reduces pain and swelling and improves quality of life measures after mandibular third molar surgery.“ J Oral Maxillofac Surg, 72(6), 1043–1048.
- Manhart, N., et al. (2002). „Administration of proteolytic enzymes bromelain and trypsin diminish the number of CD4+ cells and the interferon-gamma response in Peyer’s patches and spleen in endotoxemic balb/c mice.“ Cell Immunol, 215(2).
- Maurer, H.R. (2001). „Bromelain: biochemistry, pharmacology, and medical use.“ Cell Mol Life Sci, 58(9), 1234–1245.
- Pavan, R., Jain, S., Shraddha, Kumar, A. (2012). „Properties and therapeutic application of bromelain: a review.“ Biotechnol Res Int, 2012:976203.
- Pidard D, Frelinger AL, Bouillot C, Nurden AT. „Activation of the fibrinogen receptor on human platelets exposed to alpha chymotrypsin. Relationship with a major proteolytic cleavage at the carboxyterminus of the membrane glycoprotein IIb heavy chain. “ Eur J Biochem. 1991 Sep 1;200(2):437-47.
- Pihlstrom, B. L., Michalowicz, B. S., & Johnson, N. W. (2005). „Periodontal diseases.“ The Lancet, 366(9499), 1809-1820.
- Shah, D. and K. Mital. (2018). „The Role of Trypsin:Chymotrypsin in Tissue Repair.“ Adv Ther, 35(1).
- Šimurdová, M. (2021). „Význam Enzymelu v pooperačním ošetřování ran v horních cestách dýchacích.“ Bakalářská práce, Univerzita Karlova, 2. lékařská fakulta, Ústav ošetřovatelství, Praha.
- Smyth, S., Heron, A. (2006). „Diabetes and obesity: the twin epidemics.“ Nat Med, 12(1), 75-80.
- Tonetti, M. S., Greenwell, H., & Kornman, K. S. (2018). „Staging and grading of periodontitis: Framework and proposal of a new classification and case definition.“ Journal of Clinical Periodontology, 45(Suppl 20).
- UPV 308891: „Aplikační směs pro zvýšení účinnosti antiseptik a/nebo dezinficiens, aplikační prostředek obsahující aplikační směs, a použití této směsi.“
- Van Dyke, T. E., & Kornman, K. S. (2008). „Inflammation and factors that may regulate inflammatory response.“ Journal of Periodontology, 79(8 Suppl), 1503-1507.
- Vandooren J, Itoh Y. „Alpha-2-Macroglobulin in Inflammation, Immunity and Infections.“ Front Immunol. 2021 Dec 14;12:803244. doi: 10.3389/fimmu.2021.803244.
- Varilla, C., Marcone, M., Paiva, L., Baptista, J. (2021). „Bromelain, a Group of Pineapple Proteolytic Complex Enzymes (Ananas comosus) and Their Possible Therapeutic and Clinical Effects. A Summary.“ Foods, 10(10), 2249.